TJOD
İstanbul Şubesi



Sayın meslektaşlarım;
Nisan
ayı
toplantısı
bildiğiniz
gibi
Jinekolojide
Rutin
Endoskopi
Uygulamaları
konularını
içermektedir.
Bu
toplantıda
her
kadın
doğum
uzmanının
günlük
pratikte
uyguladığı
veya
uygulaması
gerektiği
laparoskopi
ve
histeroskopi
uygulamaları
tartışılacaktır.
Toplantının
amacı
siz
meslektaşlarımızın
bu
konudaki
bilgilerini
tazelemek
ve
endoskopik
cerrahileri
yapmayan
arkadaşlarımızı
bu
cerrahiler
için
cesaretlendirmektir.
Öncelikle
laparoskopik
cerrahiler
için
standart
pelvik
anatomi
ve
kullanmamız
gereken
enerji
modaliteleri
irdelenecektir.
Laparoskopi
sırasında
özellikle
ilk
yıllarda
en
korktuğumuz
bölüm
batına
ilk
giriş
ve
optik
trokarın
uygulaması
dır.
Bu konu ayrıntılı olarak tartışılacak ve kolaylıklar vurgulanacaktır.
Basit
histerektomi
uygulamaları
ve
myomektomi
için
hasta
seçim
ve
laparoskopik
myomektomi
bu
toplantının
önemli
konularından
biridir.
Bunun
yanında
tanısal
ve
cerrahi
histeroskopi
uygulamaları
laparoskopiden
önce
uyguladığımız
ve
daha
fazla
deneyimli
olduğumuz
işlemlerdir.
Bu
bölümde
dismorfik uterus ve Asherman sendromu gibi karmaşık konular irdelenecektir.
Sayın
meslektaşlarım
bildiğiniz
gibi
malpraktis
ve
tüketici
mahkeme
davaları
her
geçen
gün
artmaktadır.
Bu
davalara
en
sık
maruz
kalan
hekimler
grubundan
biri
de
biz
kadın
hastalıkları
ve
doğum
uzmanlarıdır.
Bu
davalara
maruz
kalmayı
azaltmanın
veya
bu
davalardan
zararsız
çıkmanın
en
önemli
yolu
bilgilerimizi
yenilemek
ve
değişen
uygulamaları
mümkün
olduğunca
takip
etmektir.
Diğer
bültenlerde
olduğu
gibi
sizlere
yardımcı
olmak
amacı
ile
yakın
zamanda
yayınlanmış
4
çalışmayı
sizlere
sunuyoruz.
Çevirileri
yapan
ve
özetleyen
arkadaşlara
teşekkürlerimizi sunuyoruz.
Bu
çalışmalardan
biri
gebelik
takibinde
sık
karşılaşılan
bir
sorun
olan
Gebelikte
Tip
1
Diyabet
Yönetimi
ile
ilgilidir.
Diğer
çalışma
ABD
tiroid
cemiyetinin,
Gebelik
ve
Postpartum
Dönemde
Tiroid
Hastalıklarının
Tanı
ve
Yönetimi
ile
ilgili
son
önerilerini
kapsamaktadır.
Bilindiği
gibi
myom
ve
myomektomi
jinekoloji
pratiğimizin
önemli
konularından
biridir.
Pek
çok
çalışma,
laparoskopik
veya
robotik
myomektomi
sonrasında
yapılan
açık
morsellasyonun
sarkom
olan
olgularda
sağ
kalım
süresini
olumsuz
yönde
etkilediğini
göstermiştir.
Son
iki
çalışma
myomektomi
sonrası
morsellasyon
ile
ilişkilidir
ve
her
iki
çalışmada
kapalı
morsellasyon
un
önemi
vurgulanmaktadır.
Ayrıca
bu
ay
İstanbul
Üniversitesi
İstanbul
Tıp
Fakültesinden
Dr.
Selin
Afşar
ve
Dr.
Samet
Topuz
’un
yazdığı
Gestasyonel
Trofoblatik
Hastalıklar
ile
ilgili
bir
derlemeyi
yayınlıyoruz.
En derin saygılarımızla
Prof. Dr. Fuat Demirkıran
Tjod İstanbul Y.K. adına

TJODist
Bülteni
Nisan 2017



TJODist
Bülteni

TJOD
İstanbul Şubesi
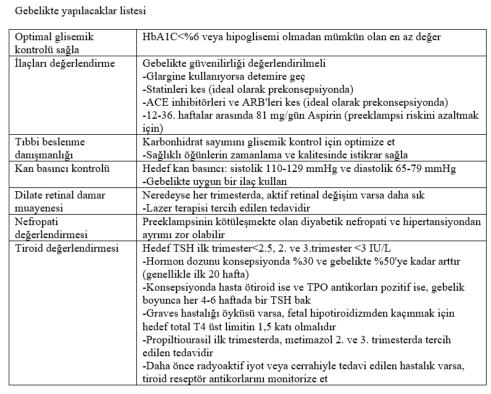
Gebelik
öncesi:
Tip
1
diyabet
(T1DM)
tüm
gebeliklerin
%0.1
-
0.2'sini
etkiler.
Gebelik
öncesi
bakımın
amaçları
HbA1c
˂%7
ve
anlamlı
hipoglisemi
olmadan
%6'ya
olabildiğince
yakın
olacak
şekilde
sıkı
glisemik
kontroldür.
Açlık
değerlerinin
80-110
mg/dl,
yemek
sonrası
1.
saat
değerlerinin
100-155
mg/dl olarak hedeflenmesi önerilir.
Kan
basıncı
hedefleri
sistolik
˂140
mmHg
ve
diastolik
˂90mmHg'dir.
Prekonsepsiyonda
kan
basıncı
kontrolü
metildopa,
kalsiyum
kanal
blokerleri
veya
bir
beta
bloker
olan
labetolol
ile
sağlanabilir.
Nefropati
serum
kreatinin
ve
idrarda
mikroalbumin
ölçümü
ile
değerlendirilmelidir.
Retinopati
muayenesi
yapılmalı
ve
proliferatif
diyabetik
retinopati
konsepsiyon
öncesi
tedavi
edilmelidir.
Otoimmün
tiroid
hastalığı
sık
olarak
eşlik
ettiğinden TSH bakılmalıdır.
Gebelik:
Erken
gebelikte
yüksek
HbA1c
en
sık
kardiyak
ve
nöral
tüp
defektleri
olmak
üzere,
artmış
konjenital
malformasyon
oranlarıyla
ilişkilidir
ayrıca
spontan
düşük,
intrauterinfetal
ölüm,
preeklampsi,
preterm
doğum
ve
perinatal
mortalitede
artış
olur.
Maternal
dolaşımdaki
aşırı
glikoz
fetal
dolaşımda,
aşırı
fetal
yağlanma
ve
LGA
veya
makrozomi
riskini
artıran
artmış
glikoz
seviyeleriyle
sonuçlanır.
Ayrıca
diyabetik
anne
bebeklerinde
fetusa
aşırı
besin
gitmesi
artmış
obezite
riski
ve
bozulmuş
glikoz
toleransı ile sonuçlanır.
İnsülin
gereksinimi
gebelik
boyunca
değişir,
ilk
9
haftada
artar,
9
-16
haftada
azalır
ve
37.
haftaya
kadar
tekrar
artar.
Gebeliğin
son
ayında
insülin
gereksinimi
genellikle
azalır.
Gebeliğin
tamamında
insülin
gereksinimi
iki
katına
çıkabilir
ve
bazal
ihtiyaçtan
prandial
insülin
ihtiyacına
doğru
bir
kayma
olur.
Amerikan
Diyabet
Derneği
kılavuzuna
göre,
gebelikte
açlık
glikozu
hedefi
60-99
mg/dl,
pik
postprandial
glikoz
hedefi
100-129 mg/dl'dir.
T1DM
hastası
gebelerin
%50'sinde,
en
Gebelikte Tip 1 Diyabetin Yönetimi
Anna Z. Feldman, Florence M. Brown
Özetleyerek tercüme eden: Dr Hakan Erenel
Cerrahpaşa Tıp. Fak. Kadın Hast. ve Doğ. Anabilimdalı Perinataloji Bilimdalı
sık
ilk
trimesterde
ve
geceleri
olmak
üzere
ciddi
hipoglisemi
gerçekleşir.
Artmış
1.saat
postprandial
kan
glikozu
nedeniyle
yemek
zamanı
insülin
dozunu
ayarlamak
yerine
bolus
dozu
arttırılan
hastalarda
görülür.
Diyabetik
ketoasidoz
gebelik
öncesine
göre
daha
düşük
glikoz
seviyelerinde
olur,
çünkü
gebelik
ketoza
eğilim
yaratan bir durumdur
Makrozomi,
neonatal
hipoglisemi
ve
respiratuar
distress,
ortalama
antepartum
glikoz
seviyelerinin
110
mg/dl
altında
olmasıyla
azaltılabilir.
Intrapartum
glikoz
seviyeleri
neonatal
hipoglisemi
açısından
antepartum
glikoz
seviyelerinden
daha
risklidir;
intrapartum
glikoz
seviyeleri
100
mg/dl'nin
altında
iken
neonatal
hipoglisemi
riski
en
azdır.
Üçüncü
trimesterde
HbA1c
%6'nın
altında
olan
kadınlarda
dahi
iri
bebek
prevelansı %25'tir. Yani çok iyi kontrollü hastalarda bile iri bebek riski fazladır.
Postpartum
Doğum
sonrası
insülin
sensitivitesinde
anlamlı
artış
olur,
bu
yüzden
dozun,
konsepsiyon
öncesi
dozun
%50'sine
düşürülmesi
tavsiye
edilmektedir.
Emziren
kadınlar
daha
düşük
bazal
insülin
dozuna
ihtiyaç
duyacaktır.
Emzirme
anne
ve
bebekler
için
oldukça
faydalıdır,
fakat
T1DM'li
kadınlar
için
insülin
sensitivitesi,
kilo
kaybı,
uyku
düzeninde
potansiyel
iyileşme
ve
anne-bebek
bağlanmasında
iyileşme
gibi faktörlerden dolayı özellikle faydalıdır
Kaynak
Feldman AZ, Brown FM. Management of Type 1 Diabetes in Pregnancy. Curr Diab
Rep. 2016 Aug;16(8):76.
Ücretsiz tam metin erişim bağlantısı:
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4919374/
TJODist
Bülteni

TJOD
İstanbul Şubesi
Giriş:
Gestasyonel
trofoblastik
hastalıklar
(GTH)
plasental
trofoblastların
anormal
proliferasyonu
ile
karakterize
birbiriyle
ilişkili
bir
tümör
grubudur
1
(Tablo
1).
Benign
GTH;
plasental
site
nodül,
egzajere
plasental
site
ve
mol
hidatiformdan
(komplet
ve
parsiyel)
oluşur
(Tablo
1).
Lokal
invazyon
ve
uzak
metastaz
yapma
potansiyelleri
mevcuttur.
Malign
olanları;
persistan
GTH
ve
gestasyonel
trofoblastik
neoplazi
(GTN)
başlığı
altında
incelenen
koryokarsinoma
(KKA),
plasental
site
trofoblastik
tümör
(PSTT)
ve
onun
bir
varyantı
olan
epiteloid
trofoblastik
tümördür
(ETT)
(Tablo
1).
Human
koryonik
gonadotropini (hCG) hastalığın tanı, takip ve tedaviye yanıtın değerlendirilmesinde kullanılır
2,3
.
Epidemiyoloji:
Epidemiyolojik
veriler;
merkezi
bir
veri-tabanının
olmaması
ve
bazı
alt
tiplerin
çok
nadir
görülmesinden
dolayı
güvenilir
değildir
4
.
Eldeki
verilere
dayanarak;
mol
hidatiformun
doğurganlık
çağında
görülen
bir
hastalık
olduğu
ve
insidansının
farklı
coğrafik
bölgelerde
%0,6-2
arasında
olduğu
söylenebilir
5-7
.
Bu
coğrafik
değişime
rağmen;
molar
gebelik
riski etnik, ırksal veya kültürel farklılık göstermemektedir
8,9
.
Etyoloji:
Diyette
A
vitamini
(karoten)
ve
hayvansal
yağlardan
fakir
beslenenlerde
komplet
molar
gebelik
riski
arterken
parsiyel
molar
gebelik
insidansında
bir
artış
izlenmemektedir
10,11
.
İnfertilite
ve
spontan
düşük
hikayesi
bulunanlarda
2-3
kat
artmış
bir
molar
gebelik
riski
vardır
12
.
Komplet
molar
gebelik
için
en
önemli
iki
risk
faktörü;
anne
yaşı
ve
geçirilmiş
molar
gebelik
öyküsüdür
13
.
16
yaş
altı
ve
40
yaş
üstü
kadınlarda
(5-10
kat)
komplet
molar
gebelik
riski
oldukça
artmıştır
ve
bu
risk
50
yaş
üstünde
her
3
gebelikten
birinin
molar
gebelikle
sonlanmasına
yol
açar
14,4
.
İleri
anne
yaşı
parsiyel
molar
gebelik
için bir risk faktörü değildir
13
.
Ailesel
tekrarlayan
mol
hidatiform;
19.
kromozom
üzerindeki
NLRP7
lokusunda
kayıp
(missense)
mutasyon
sonucu
oluşur
13
.
Geçirilmiş
iki
molar
gebelik
öyküsü
olanlarda
mutasyonun
%60-70
(+)
olduğu
bildirilmiştir
15
.
Mutasyona
uğrayan
gen maternal sessizleşme (imprinting) sonucu tekrarlayan komplet molar gebeliğe yol açar
16
.
Persistan
GTH,
mol
boşaltılması
sonrası
%15
oranında
izlenir.
Koryokarsinom
50000
gebelikte
bir
görülür
17
.
İleri
anne
yaşı,
geçirilmiş
molar
gebelik
ve
A
kan
grubu
taşıyıcılığı
riski
arttırır
9
.
PSTT
ve
ETT
oldukça
nadir
görülen
formlar
olup,
%95
term
bir gebeliği veya non-molar düşüğü takiben aylar hatta yıllar sonra görülebilir
18
.
Patogenez:
GTH
patogenezinde
genetik
sessizleşmenin
önemli
bir
yeri
vardır
19
.
Genetik
sessizleşme
gametogenez
sırasında
oluşur
ve
şimdiye
kadar
yaklaşık
80
gende
tespit
edilmiştir.
Maternal
genetik
sessizleşmede
sadece
paternal
genler
eksprese
edilir
20
.
Kabaca
paternal
genler
plasental
büyüme
üzerinde
etki
gösterirken
maternal
genler
fetal
büyüme
üzerinde etkilidir.
Yoğun
paternal
gen
varlığında
yoğun
trofoblastik
proliferasyon
oluşur.
Molar
hastalığın
malignite
potansiyeli
heterozigosite
(2
farklı
sperm
ile
döllenme)
ve
homozigosite
(1
sperm
ile
döllenme
ve
duplikasyon)
ile
farklılık
gösterir.
Y
kromatin
varlığı
arttıkça
malignite
potansiyeli
de
artmaktadır.
Molar
gebeliklerde
%9,
invazif
molar
gebelikte
%50
ve
koryokarsinomda
%74
oranında Y kromatini tespit edilmiştir
19,20
.

GESTASYONEL TROFOBLASTİK HASTALIKLARDA YÖNETİM
Op. Dr Selim Afşar, Prof Dr Samet Topuz
İstanbul Üniversitesi, İstanbul Tıp Fakültesi,
Kadın Hastalıkları ve Doğum Anabilim Dalı, Jinekolojik Onkoloji Bilim Dalı


TJODist
Bülteni

TJOD
İstanbul Şubesi

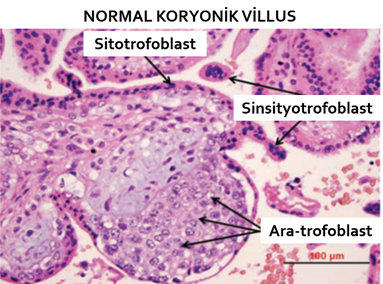
Trofoblastik farklılaşma ve GTH
GTH
blastokistin
en
dış
tabakasını
oluşturan
trofoektodermde
yerleşen
plasental
trofoblastlardan
gelişir
21
.
Trofoblastik
doku;
sitotrofoblast,
sinsityotrofoblast
ve
intermediate
trofoblastlardan
oluşur
(Şekil
1).
Sinsityotrofoblastlar
endometrial
stromayı
invaze
eder
ve
başlıca
hCG
salgılanmasından
sorumludur.
Sitotrofoblastlar
ise
sinsityotrofoblastlar
ile
birleşerek
koryonik
villus
yapısını
oluşturur.
Villüs-dışı
sitotrofoblastlar
intermediate
trofoblastlara
farklılaşarak
spiral
arter
duvarını
invaze
ederler
21,22
.
Çoğu
GTH
(parsiyel
mol
hariç)
fetüsten
kaynaklanır
ve
sadece
paternal
genetik
materyal
(androgenetik)
içerir
21
.
Şekil 1. Sitotrofoblast, sinsityotrofoblast ve ara trofoblastların fotomikrografı
21
.
Üç
farklı
trofoblast
tipide
çoğalarak
GTH
oluşturabilir
23
.
Trofoblastların
içerdiği
farklı
tipteki
antijenler
immünohistokimyasal
incelemeyle tespit edilerek GTH ayırıcı tanısında ve patogenezinin aydınlatılmasında kullanılabilir
24
(Tablo 2).
1. Egzajere Plasental Site
Endometriyum
ve
myometriyumun
invazif
intermediate
trofoblast
ile
yoğun
infiltrasyonu
sonucu
oluşur,
sıklıkla
uterin
küretaj
ve
histerektomi
materyallerinde
insidental
olarak
tespit
edilir
25
.
Endometriyal
stroma
ve
glandlarda
destrüksiyon
izlenmez.
Normal
gebelik
veya
1.
trimester
düşüklerinden
sonra
görülür.
Gerçek
bir
lezyondan
daha
çok
abartılı
fizyolojik
bir
yanıtı
gösterir.
Plasenta
normal
olarak
izlenir
ve
trofoblastlarda
mitotik
aktivitenin
yokluğu
PSTT
ile
ayrımında
önemli
bir
ipucudur. PSTT benzer şekilde hPL ve Mel-CAM için diffüz boyanma gösterirken PLAP için fokal pozitiflik gösterir
22
………
Tüm makale için tıklayınız


TJODist
Bülteni

TJOD
İstanbul Şubesi
Morcellation worsens survival outcomes in patients with undiagnosed uterine
leiomyosarcomas: A retrospective MITO group study.
Francesco Raspagliesi, M.D., Giuseppa Maltese, M.D., Giorgio Bogani, M.D., Ph.D., Giovanni Fucà, M.D., Stefano Lepori, M.D.,
Pierandrea De Iaco, M.D., Myriam Perrone, M.D., Giovanni Scambia, M.D., Gennaro Cormio, M.D., Stefano Bogliolo, M.D., Alice
Bergamini, M.D., Giuseppe Bifulco, M.D., Paolo Giovanni Casali, M.D., Domenica Lorusso, M.D., Ph.D.
Özetleyerek Tercüme Eden: Op. Dr. Hasan Turan,
Cerrahpaşa Tıp Fakültesi Kadın Hastalıkları ve Doğum AD, Jinekolojik Onkoloji BD.
ÖZET
Amaç:
Tanımlanmamış uterin sarkomlarda morselasyonun sağkalım üzerindeki etkilerini araştırmak
Metod:
MITO
grubuna
dahil
olan
8
referans
merkezinde
yapılan
retrospektif
bir
çalışmadır.
Benign
myoma
uteri
nedeniyle
morselasyon
yapılıp
,nihai
patoloji
sonucunda
evre
I
uterin
sarkom
tanısı
alan
kadınların
verileri,
morselasyon
yapılmayan
kadınlarınki
ile
karşılaştırıldı.Uterin
sarkoma
dahil
edilen
patolojiler:
leiyomyosarkomalar
(LMS),
malignite
potansiyeli
belirsiz
düz
kas
tümörleri
(STUMP),
düşük-dereceli
endometriyal
stromal
sarkomlar
(LG-ESS)
ve
andiferansiye
uterin
sarkomlar (UUS). İki yıllık sağkalım sonuçları Kaplan-Meir ve Cox modelleri kullanılarak değerlendirildi.
Bulgular:
Toplam
125
hasta
çalışmaya
alındı:
31(%24.8)
hastaya
laparoskopik
enerji
ile
morselasyon,
21(%16.8)
hastaya
açık
cerrahide
enerjisiz
morselasyon
uygulanırken,
açık
cerrahi
yapılan
73(%58.4)
hastaya
morselasyon
ugyulanmadı.
LMS
tanısı
alan
hastalar
dikkate
alındığında
morselasyon,
hastalıksız
sağkalım
ile
ilişkilendirilememiştir.
Buna
rağmen
enerjili
ya
da
enerjisiz
morselasyon
yapılan
hastaların
ölüm
oranı
morselasyon
yapılmayanlara
göre
3
kat
artmıştır
(p=0.02).
Morselasyonun,
STUMP
tanısı
alan
hastalarda
ise
rekürrens
insidansını
arttırdığı
gözlenmiştir
(HR
7.7,
p
=
0.09);
LG-ESS ve UUS tanısı alan hastalarda ise morselasyonun sağkalım sonuçları üzerinde etkisi gözlenmemiştir.
Sonuçlar:
Bizim
verilerimize
göre
morselasyon
tanımlanmamış
LMS’da
ölüm
riskini
arttırmaktadır.
Benign
olduğu
görülen
uterin
myomlarda
enerjili
morselasyonun
yarar-zarar
oranını
değerlendirmek
için
daha
fazla
prospektif
çalışmaya
ihtiyaç
vardır.
1. Giriş
Uterin
LMS
nadir
bir
durum
olup
bütün
uterin
malignitelerinin
%1.5’i
kadardır,
tahmini
yıllık
insidansı
0,64/100.000
kadındır
[1].Andiferansiye
karsinom
sınıfındaki
karsinosarkomlar
dışlandığında
uterin
sarkomların
%70’i
LMS
ve
%30’u
stromal
sarkomlardır
[2].
LMS
tanısı
alan
hastaların
sağ
kalımı,
tanı
zamanındaki
evresiyle
güçlü
ilişki
göstermektedir:
Evre
I
tümörlerin
5
yıllık
sağ
kalım
oranı
%84,3
,bu
durum
evre
II’de
(%43,6)
,
evre
III’te
(%38,8)
ve
evre
IV’te
(%19,8)
dramatik
olarak
düşmektedir
[2].
Preoperatif
olarak
benign
myoma
uteri
ile
uterin
sarkomları
ayırt
etmek
zor
olabilir.
Myoma
uteri
olduğu
düşünülen
vakalar
içindeki
sarkomların
gerçek
prevalansı
tam
olarak
bilinmemektedir,
retrospektif
verilere
dayalı
metaanalizlerde
geniş
bir
aralıktan
(%0.45–0.014)
bahsedilmektedir
[3,4].
Bunun
yanında
her
ne
kadar
bazı
hasta
özellikleri
(ileri
yaş,
semptom
varlığı)
ve
uterin
kitlelerin
görüntülemelerdeki
morfolojik
özellikleri
uterin
sarkom
yönünde
düşündürse
de
güvenilir
bir
ayırıcı
tanıya
gitmek
zordur
[5].
FDA,
enerjili
morselasyona
karşı
olarak
Kasım
2014’te
bir
güvenlik
tebliği
yayınladı; morselasyon, tanımlanmamış uterin sarkomdaki olası zararlı etkileri nedeniyle önerilmiyordu [6].



TJODist
Bülteni

TJOD
İstanbul Şubesi
Myom
olarak
düşünülen
bir
kitlenin
sarkom
(veya
başka
bir
malignite)
olduğu
kanıtlanırsa,
tümörün
bütünlüğünü
bozan
her
hangi
bir
morselasyon
yöntemi
muhtemelen
hastalığın
evresini
ilerletip
sağkalımı
etkileyecektir.
Enerjili
morselasyon
yönteminde silindirik bıçağın hareketleri tümör hücrelerinin peritona ‘ekilme’ olgusunu açıklamaktadır [7].
Bundan
sonra
bu
konu
ile
ilgili
olarak
pekçok
bilimsel
merkez
kendi
görüşünü
yayınlayarak
enerjili
morselasyonun
kullanımını
önerecek
sağlam
bilimsel
verilerin
olmadığı
sonucuna
ulaşmışlardır
[8].
Bu
retrospektif
çalışmada,
tanı
almamış
uterin
sarkomların
onkolojik
sonuçlarını
,MITO
(Multicentre
Italian
Trialists
in
Ovarian
Cancer
and
Gynecologic
Malignancies)
grubuna
dahil
olan
8
referans
merkezinde,
morselasyon
yapılan
kadınlar
ile
morselasyon
yapılmayan
kadınları karşılaştırarak belirlemeye çalıştık.
2. Materyal ve Metod
MITO
grubuna
dahil
olan
8
merkezde
opere
olmuş
olguların
değerlendirildiği
retrospektif
bir
çalışmadır.
Ocak
2004
ile
Aralık
2014
tarihleri
arasında
benign
myoma
uteri
nedeniyle
opere
olup,
nihai
patoloji
sonucu
uterin
sarkom
olan
kadınların
tıbbi
kayıtları
incelendi.
Çalışmaya
dahil
edilen
tüm
hastalardan
veri
toplanması
ve
bilimsel
çalışma
için
kişisel
verilerinin
kullanılması ile ilgili yazılı onam alındı.
Dahil
edilme
kriterleri:
(1)
benign
uterin
kitle
için
cerrahi
yapılan
hastalar,
(2)
nihai
histolojik
tanısı
evre
I
uterin
sarkom
olanlar
ve
(3)
18
yaş
ve
üstü
hastalar.
Dışlanma
kriterleri:
onamın
verilmemesi
ve
5
yıl
içinde
diğer
bir
kitlesel
malignite
tanısı
almış
olmak.
Çalışmanın
birincil
hedefi
morselasyon
yapılan
kadınların
sağkalım
sonuçları
ile
hastalıksız
sürelerini
,morselasyon yapılmayanlarla karşılaştırarak değerlendirmekti.
Benign
myomlar
(daha
sonra
beklenmedik
bir
şekilde
sarkom
olduğu
kanıtlanan)
için
morselasyon
yöntemi
ile
myomektomi
veya
histerektomi
yapılan
kadınların
verileri
,benzer
klinik
bulguları
olan
fakat
morselasyon
yapılmayan
kadınlarınki
ile
karşılaştırılarak
değerlendirildi.
Eğer
cerrahlar
preoperatif
veya
peroperatif
notlarında
herhangi
bir
malignite
şüphesinde
bulunmadıysa
uterin
sarkomlar
‘beklenmedik’
olarak
kabul
edildi.
Tanımlamalar
oluşturulduktan
sonra
veriler
tıbbi
kayıtlardan
edinildi;
kadınların
demografik
bilgileri,
ameliyat
raporları,
nihai
patoloji
sonuçları
incelendi.
Toplanan
diğer
bilgiler;
ameliyat
endikasyonu,
preop
değerlendirme
ayrıntıları,
son
tanıdan
sonra
adjuvan
tedavi,
rekürensin
zamanı
ve
yeri
ile
ölüm
tarihi
olarak
belirlendi.
Hastalığın
evresi
ile
histolojik
sınıflaması
sırasıyla
FIGO
[9]
ve
WHO
[10]
sistemleri
kullanılarak
değerlendirildi.
LMS,
STUMP,
LG-ESS
ve
UUS
uterin
sarkom
olarak
ele
alındı.
Takipler
pelvik
muayene
ve
ultrasonografi
ile;
ilk
iki
yıl
3
ay
arayla
,sonraki
3
yıl
6
ay
arayla
ve
sonrası
için
de
yıllık
olarak
yapıldı.
Batın
içi
herhangi
bir
rekürrens
peritoneal
yüzey
ile
ilişkilendirilirken
;
karaciğer,dalak
ve
akciğer
parankimi
metastazları
uzak
rekürrens
olarak
kabul edildi.
2. 1. İstatistiksel analiz
İstatistiksel
analiz
GraphPad
Prism
version
6.0
for
Mac
(GraphPad
Software,
San
Diego
CA)
ve
IBM-Microsoft
SPSS
version 20.0 kullanılarak yapıldı.
3. Sonuçlar
Çalışmaya
katılan
8
merkezde
10
yıllık
süreçte
benign
myomlar
nedeniyle
4000
cerrahi
girişim
yapıldı.
Bunlar
arasında,
beklenmedik
bir
şekilde
FIGO
evre
I
uterin
sarkom
tanısı
alan
125
hasta
(%3,1)
belirlendi:
52
hastaya
(%41,6)
morselasyon uygulanmış olup 73 hastaya (%58,4) uygulanmamıştır.
Ortalama
yaş
55
olup
kadınların
çoğunda
(%72,8)
uterin
LMS
mevcuttu.
Morselasyon
yapılan
hastaların
çoğunda
(n=31;%59,6)
cerrahi,
laparoskopik
olarak
uygulandı.
21
hastada
(%40,3)
açık
abdominal
cerrahi
sırasında,
büyük
uterus
veya
perop
teknik
problemler
sebebiyle,
uterin
morselasyon
uygulandı.
Morselasyon
yapılanlar
ile
yapılmayanlarda
adjuvan
tedavi
alan
hastaların
prevalansı
benzerdi
(
sırasıyla
%57,7
vs.
%67,1),
(OR:
1,49;
%95
CI:0,71-0,32;
p=0,34).
Vakaların
büyük
bir
kısmında
(%93,6)
adjuvan
tedavi
kemoterapi
olarak
uygulandı.
Sarkomların
histolojik
tiplerinin
tamamen
farklı
biyolojik ve klinik özellikleri sebebiyle farklı tümörleri ayrı ayrı analiz etmeye karar verdik.
3.1. Tanı almamış leiyomyosarkomların morselasyonu
3.1.1.
Leiyomyosarkomlar(LMS):
LMS
grubunda
morselasyonun
2
yıllık
hastalıksız
sağkalıma
etkisinin
olmadığı
tespit
edildi
(HR:1,09;
CI
%95:0,58-2,02;
p=0,79).
Buna
rağmen
morselasyon
(enerjili
ya
da
enerjisiz)
yapılan
hastalarda
ölüm
riski
3
kat
artmış
bulundu
(HR
3.0;
CI
%95:
1.15-7.91;
p
=
0.02)
(Fig.
1).
Tek
değişkenli
analizde
enerjili
morselasyonun
hasta
prognozunu
etkileyen
tek
faktör
olduğu;
açık
abdominal
cerrahide
morselasyonun
ortalama
sağkalımı
etkilemediği
tespit edildi. Buna rağmen çoklu analizde sadece enerjili morselasyon bağımsız olarak sağkalım ile ilişkili bulundu.
3.1.2.
LMS:
Laparoskopik
enerjili
morselasyonyapılan
olgular
ile
açık
abdominal
cerrahide
morselasyon
yapılmayan olguların karşılaştırılması
Laparoskopik
enerjili
morselasyon
yapılan
hastalar
ile
açık
cerrahide
morselasyon
yapılmayan
hastalar
karşılaştırıldığında
iki
yıllık
ortalama
sağkalım
(HR:
1.03;
CI
%95:
0.49
-
2.13;
p
=
0.82)
ve
hastalıksız
sağkalım
(HR:
1.79;
CI
%95:
0.74
-
5.25; p = 0.20) açısından fark bulunmadı.

TJODist
Bülteni

TJOD
İstanbul Şubesi
Buna
rağmen
enerjili
morselasyon
yapılan
hastalarda
nükse
kadar
olan
süre
daha
kısa
bulundu
(enerjili
morselasyon
yapılanlarda
5
ay,
morselasyon
yapılmayanlarda
12
ay
,
HR
1.1;
CI
%95:
0.5730
–2.165;
p
=
0.75).
Bu
nedenle
hastalığın
nüks
ettiği
yeri
analiz
ettik:
enerjili
morselasyon
yapılanlarda
,
morselasyon
yapılmayan
hastalara
göre,
peritoneal
nüksler
daha
sık
bulundu
(%66,6
vs.
%39,2
sırasıyla,
OR
1.67
CI
%95:
0.52
-
5.29;
p
=
0.38).
Enerjili
morselasyon
yapılanlar
,morselasyon
yapılmayanlar
ile
karşılaştırıldığında
daha
yüksek
ölüm
riski
mevcuttu
(HR
3.0,
CI
%95:
1.10
-8.11;
p
=
0.02);
benzer
şekilde,
ortalama
sağkalım
enerjili
morselasyon
yapılanlarda
daha
kısaydı
(23
vs.
36
ay
sırasıyla;
HR
2.9
CI
%95:
1.20 - 9.12; p = 0.02).
3.1.3. LMS: açık abdominal cerrahide morselasyon yapılan ile yapılmayan olguların karşılaştırılması
Sadece
açık
abdominal
cerrahi
yapılan
hastalar
ele
alınarak
,enerjisiz
morselasyon
yapılanlar
ile
morselasyon
yapılmayanlar
karşılaştırıldığında
hastalıksız
sağkalım
(HR:
1.31;
CI
%95:
0.54
-
3.09;
p
=
0.56)
ve
ortalama
sağkalım
(HR: 1.64; CI %95: 0.39 - 8.17; p = 0.44) açısından fark bulunmamıştır.
.
3.2. Tanı almamış diğer uterin sarkomların morselasyonu
Diğer
histolojik
alt
tiplere
bakıldığında,
bütün
karşılaştırmalar
hasta
sayılarının
azlığından
dolayı
eksik
kalmaktadır;buna
rağmen
morselasyon
yapılan
STUMP
olgularında
anlamlı
olmasa
da
hastalıksız
sağkalımda
kısalma
eğilimi
mevcuttur
(HR
7.71;
CI
%95:
0.79
-
75.12;
p
=
0.09);
LG-ESS
ve
USS
ele
alındığında
sağkalım
sonuçlarında
herhangi
bir
fark
tespit
edilmemiştir.
4. Tartışma
Retrospektif
ve
çok-merkezli
olan
bu
çalışma,
beklenmedik
LMS
tanısı
alan
hastalarda,
morselasyonun
onkolojik
sonuçlar
üzerindeki
olumsuz
etkilerini
doğrulamaktadır.
Bizim
verilerimiz,
morselasyon
yapılıp
LMS
tanısı
alan
hastalarda,
morselasyon yapılmayan hastalara göre, 3 kat daha yüksek ölüm riski olduğunu göstermektedir.
Yakın
zamanda
FDA,
beklenmedik
sarkom
vakalarında
morselasyonunun
prognostik
etkisi
ile
ilgili
uyarıda
bulunmuştur.
FDA’in
uyarısı,
morselasyonun
batın
içi
rekürrens
ve
ölüm
riskini
arttırdığına
dair
verileri
içeren
retrospektif
çalışmaların
analizine dayanmaktadır [11,12,13].
Klinik
uygulamalarda
büyük
bir
değişiklik
yapmış
olsa
da
(yaklaşık
10
klinisyenin
8’i
benign
myomlar
nedeniyle
yapılan
histerektomilerde
değişikliklere
başvurmuştur
)
[14],
FDA
önerisi,
retrospektif
çalışmalardan
elde
edilen
düşük
dereceli
kanıt düzeyinden dolayı eleştirilmektedir ve birkaç otorite, daha sağlam verilerin gerekliliğini vurgulamaktadır.
Jinekolojik
maligniteler
için
referans
olan
8
merkezin
tecrübesine
dayanarak
yapılan
çalışmamızda,
LMS
tanısı
olup
morselasyon
yapılan
hastalar,
uterusu
parçalanmadan
çıkartılan
hastalar
ile
karşılaştırıldığında,
morselasyon
yapılan
olgularda
,ortalama
sağkalımın
kısaldığı
ve
ölüm
riskinin
3
kat
arttığı
görülmektedir.
Morselasyon
sağkalım
için
tek
bağımsız
olumsuz
risk
faktörü
olarak
karşımıza
çıkmıştır.
Literatür
ile
benzer
şekilde[15]
bizim
çalışmamızda
da
uterin
morselasyona
bağlı
tümör
yayılımının,
adjuvan
tedavi
yöntemleri
ile
dengelenemediği
gösterilmiştir.Bu
çalışmada
enerjili
morselasyon
ile
açık
abominal
morselasyon
yapılan
hastaları
ayrı
ayrı
değerlendirdik.
Aslında,
açık
cerrahide
morselasyonun
daha
zor
vakalarda
(ve
büyük
ihtimalle
ileri
hastalık
aşamasındaki
vakalarda)
yapıldığını
söyleyebiliriz.
Bu
nedenle
olası
yanılgıları
azaltmak
için
enerjili
morselasyon
tek
başına
çalışıldı.
Bizim
verilerimiz
açık
abdominal
cerrahi
yapılan olgular dışlandığında bile laparoskopik yapılan enerjili morselasyonun olumsuz bir faktör olduğunu göstermiştir.
Uterin
sarkom
şüphesiyle
cerrahi
yapılan
hastalar
ile
ilgili
çalışmalar,
uterin
LMS’un
4
hastadan
1’inde
tanı
aldığını
göstermiştir.
Bu
da
benign
görünümlü
kitlelerde
uterin
sarkom
insidansının
<%1
olduğunu
ama
LMS
olduğundan
şüphelenilen
kitlelerde
bu
oranın
%20-25’e
çıktığını
öne
sürmektedir.
Diğer
bir
görüşe
göre,
parçalanmış
örneklerin
patolojik
incelenmeye
uygun
olmaması,
morselasyon
yapılan
hastalarda
eksik
ya
da
gecikmiş
tanıya
sebep
olarak
prognozun kötüleşmesine katkıda bulunmaktadır. [22 -23].
Biz
de
belirtmek
zorundayız
ki
benign
lezyonlarda
bile
morselasyon
tamamen
risksiz
değildir.
Laparoskopik
morselasyondan
sonra
iatrojenik
olarak
küçük
boyutlu
doku
parçalarının
ekilmesi
parazitik
myomların
peritoneal
kavitede
gelişmesine
sebep
olmaktadır
[24].
Park
ve
ark
ile
Oduyebo
ve
ark’a
göre
aynı
durum
düşük
riskli
düz
kas
tümörlerine
de
uyarlanabilir
[25,26].
Bizim
verilerimiz
morselasyonun;
istatistiksel
anlamlılık
olmasa
da,
LG-ESS’da
ve
STUMP’ta
hastalıksız
sağkalım
süresini
kısalttığı
yönündedir.
Ancak
ortalama
sağkalımı
etkilememektedir.
Ortalama
sağkalım
üzerinde etkisinin olmaması, nüksün başarılı bir şekilde cerrahi olarak tedavi edilmesi ile açıklanabilir.
Bu
çalışmanın
kısıtlılığı
retrospektif
çalışma
olmasından
kaynaklanmakatadır.
Takip,
cerrahi
yaklaşım,
adjuvan
tedavi
ile
ilgili
heterojen
olması
ve
en
önemlisi
bu
kadar
nadir
hastalığın
küçük
bir
örnekleminin
olması
çalışma
ile
ilgili
diğer
kısıtlılıklardır.
Uzun
süreli
izlemde
tanı
araçlarındaki
ve
cerrahi
yaklaşımdaki
değişkenlikler
diğer
olası
yanılmalara
sebep
olabilir.

TJODist
Bülteni

TJOD
İstanbul Şubesi
Buna
rağmen
bizce
iki
konuya
değinilmelidir:
1.
Son
iki
dekadda
minimal
invaziv
cerrahi
bazı
jinekolojik
hastalıklar
için
altın
standart
hale
gelmiştir.
2.
Uterin
sarkomlar
düşük
prevalansa
sahiptirler
ve
hiçbir
tanı
koydurucu
patognomonik
özellikleri
yoktur.
Bu
iki
karşıt
durumu
ortak
noktada
birleştirmek
için
tanı
araçlarının
doğruluğunu
arttırmak
ve
batın
içi
morselasyondan
kaçınmaya
yönelik
stratejiler
(torba
içinde
morselasyon,
kitlenin
minilaparatomi
veya
vaginal
yoldan
posterior
kolpotomi
ile
çıkarılması
gibi)
geliştirmek
gerekmektedir.
[27,28].
Uterin
sarkom
tanısı
koymak
için
pekçok
tahminden
oluşan
skorlama
sisteminin
geliştirilmesi
tanı
açısından
ilginç
bir
öneridir:
PREoperatif
Sarkom
Skoru
(PRESS)
[29]
yaş,
serum
laktat
dehidrojenaz
düzeyi
ve
endometriyal
sitolojik
bulgular
ile
MRI
bulgularını
içermektedir.
Tanı
doğruluğu %84, pozitif prediktif değeri %63, negatif prediktif değeri %93, sensitivitesi %80, spesifitesi %85’tir [30].
Hastaların
laparoskopik
cerrahi
için
klinik
olarak
değerlendirilmesi
belirleyicidir:
özellikle
şüpheli
leiomyomu
olan
hastalarda
batın
içi
morselasyondan
kaçınılmalıdır.
Ek
olarak,
güvenilir
tanı
koymayı
sağlayacak
yeterli
aracın
yokluğu
sebebiyle
bütün
hastalar
tanı
almamış
uterin
sarkom
açısından
göz
önünde
bulundurulmalı
ve
mevcut
güncel
bilgilere
dayanarak
,hastalardan detaylı aydınlatılmış onam alınmalıdır.
Makale linki: https://www.ncbi.nlm.nih.gov/pubmed/27817933



TJODist
Bülteni

TJOD
İstanbul Şubesi
Özet:
Nadir
görülen
okült
sarkomlarda
kapalı
sistem
içerisinde
yapılmamış
morselasyon
düşük
sağkalım
ile
ilişkili
bulunmuştur.
Uterus
ve
miyom
morselasyonu;
iatrojenik
endometriosis,
parazitik
miyom
ve
nadir
de
olsa
yaygın
peritoneal
leiyomiyomatozise
neden
olabilir.
Bu
benign
olgular
sarkomatöz
dokunun
malign
yayılımından
daha
sık
görülür.Minimal
invaziv teknikle uygulanan kapalı sistem içerisinde morselasyon karın boşluğu içerisine doku yayılımını engelleyebilir.
Giriş:
Fibroid
veya
uterin
miyom
kadın
genital
sistem
benign
tümörlerinin
en
sık
görüleni
olup
50
yaş
civarındaki
kadınlarda
%70
görülebilir (1). Çoğu miyom asemptomatik olsa da, %15-20’si semptomatik olabilir (2).
Morselasyon,
miyomektomi,
supraservikal
(veya
subtotal)
histerektomi
veya
total
histerektomi
sırasında
büyük
spesimenler
çıkartılırken
dokunun
küçük
parçalara
ayrılmasıdır.
İlk
elektrikli
morselatör
1993
yılında
tanıtıldı,
1995
yılında
FDA
tarafından
onaylanarak
doku
kaybı
önlenerek
operasyon
süresi
kısaltılmış
oldu
(6).
Ancak
2014’te
morselasyon
sonrası
gelişen okült leiyomiyosarkom vakası sonrası FDA enerjili morselatörleri önermediğini bildirdi (7).
Bu
derleme
ile,
uterus
veya
miyom
morselasyonu
ile
ilişkili
malign
ve
benign
risklere
odaklanarak,
bunların
klinik
pratiğe
ektikleri ve kapalı sistem içerisinde yapılmayan enerjili morselasyonun alternatiflerini değerlendirdik.
Metod:
Elektronik
ortamda
şu
veri
tabanlarını
kullandık:
Pubmed,
EMBASE,
Ovid
MEDLİNE,
Google
Scholar
ve
Cochrane
.
Anahtar
kelimeler:
morsellasyon:
sarkom:
leiomiyosarkom:parasitik
miyom:
uterin
miyom:
uterin
fibroid:
laparoskopik
miyometkomi:
laparoskopik
total
histerektomi:
ve
laparoskopik
supraservikal
histerektomi.’Eylül
2016ya
kadar
yayınlanmış
İngilizce yayınlar ile sınırlandırılıdı. İki yazar bağımsız olarak değerlendirdi.
Okkült Uterin Kanser Morselasyonu:
Morselasyonun
en
ciddi
etkisi,
peritoneal
boşluğa
malign
hücrelerin
yayılımıdır.
Bu
durum
batın
irrigasyonuna
rağmen
gelişmektedir.
3.1. Endometrial kanser:
Uterin
malignitelerin
%95’
i
endometrial
kanserlerdir.
Cerrahi
öncesinde
endometrial
örnekleme
yapılarak
tespit
edilebilir
(8).
Miyomu
öntanısıyla
opere
edilen
kadınlarda
cerrahi
sonrasında
endometrial
karsinom
prevalansı
%
0-0,53
arasında
değişmektedir.
3.2. Uterin Sarkom
Uterin
malignitelrin
%5’ini
oluşturur
ve
en
sık
görüleni
leiyomiyosarkomdur
(8).
Endometrial
karsinomun
aksine,
spesifik

Jinekolojik Laporoskopik Cerrahide Kapalı Sistem İçerisinde Yapılmamış
Morselasyonun Uzun Dönem Etkileri
Özetleyerek Tercüme Eden: Op. Dr. Hasan Turan,
Cerrahpaşa Tıp Fakültesi Kadın Hastalıkları ve Doğum AD, Jinekolojik Onkoloji BD.


TJODist
Bülteni

TJOD
İstanbul Şubesi
olmayan bulgular ve uterin miyoma benzer semptomlar nedeniyle preoperatif uterin sarkom tanısı koymak zordur.
Okült
leiyomiyosarkom
riski
değerlendirilirken,
uterin
morselasyon
yapılmış
kadınları
değerlendirmek
önemlidir.
Lieng
ve
ark’nın
(17)
yaptığı
çalışmada,
uterin
miyom
öntanısıyla
yapılan
histerektomilerde,
6
kadında
histerektomi
sonrasında
okült
uterin
sarkom
saptandı
(%0.12),
bu
çalışmada
morelasyon
ile
ilişkili
leiyomyosarkom
riski
1/4771
olarak
saptandı.Diğer
çalışmalar
incelendiğinde
ise
uterin
morselasyona
bağlı
okült
uterin
sarkom
prevalansı
%0.05
-0.6
arasında
değişmektedir
(18-20).
3.3. Tümör yayılımı
Malign
dokuda
morselasyonun
en
büyük
endişesi;
doku
bozulması
ve
yayılımının
rekürrens
ve
sağkalıma
olan
etkisidir.
Diğer
endişeler;
uygun
tanı,
evreleme
ve
derecelendirmede
ortaya
çıkan
zorluklardır
(21).
Seidman
ve
ark.
,
okült
uterin
kanser
morselasyonu
sonrası
tümör
yayılımını
değerlendirdikleri
çalışmalarında
,
leiomiyosarkom
tanısı
alan
7
olgunun
4’ünde
second
look
laparoskopi
sonrasında
tümör
yayılımı
saptadı.
2’si,
Primer
cerrahiden
en
az
13
ay
sonra
tanı
aldı.
Bu
vakalar, yayılımdan çok hastalık rekürrensi şeklinde olabileceğini göstermektedir (22).
Oduyedo
ve
ark.
uterin
leiomiyosarkom
veya
malignite
potensiyeli
belirsiz
düz
kas
tümörlerinde
(STUMP)
morselasyon
sonrası
abdominal
reeksplorasyonun
önemini
araştırdılar
(23).
Primer
cerrahi
ve
reekplorasyon
arasında
ortalama
33
gün
vardı.
Evre
1
leiyomiyosarkom
veya
STUMP
tanısı
almış
11
hastada
reeksplorasyon
sonrası
yaygın
peritoneal
hastalık
sırasıyla %28,6 ve %25 oranlarında saptandı.
3.4. Sağkalıma olan etkileri
Uterin
kanserde
morselasyonun
sağkalım
ve
rekürrens
üzerine
etkisi
pek
çok
çalışmada
değerlendirilmiştir.
Cerrahi
sırasında
leiyomiyosarkomun
parçalanmasının
etkisini
araştıran
retrospektif
bir
çalışmada
total
histerektomi
ile
sağkalımda
artış
ve
rekürrensin
azaldığı
tespit
edilmiştir
(24).
Benzer
bir
çalışmada,
Parjk
ve
ark.
25
morsele
leiomiyosarkom
ve
31
total
abdominal
histerektomili
kadını
karşılaştırmıştır
(25).
Cerrahi
sırasında
tümör
morselasyonu
abdominopelvik
yayılım
riskini arttırken (%44 vs. %12.9, p=0,032) sağkalım süresini olumsuz etkilemiştir.
125
okült
leiyomiyosarkomlu
vakadan
oluşan
geniş
popülasyonlu
kohort
çalışmasında,
sağkalım
oranları
ve
rekürrens
oranları
enerjili
morselasyon
yapılan,
enerjisiz
morselasyon
yapılan
ve
morselasyon
yapılmayan
gruplarda
değerlendirilidi
(26).
Morsele
edilmeyen
gruba
göre
morsele
edilen
grupta
birinci
yılda
mortalite
oranı
artmştır
(26)
.
202
hastadan
olşan
bir
metaanalizde
ise
okült
leiyomiyosarkomda
morselasyon
ile
rekürrens
ve
ölüm
oranlarında
artışta
belirgin
korelasyon
olduğu bildirilmiştir (27).
4. Morselasyonun malign olmayan etkileri
2004
FDA’in
uyarısı
ile,
uterus
morselasyonu
sırasında
malign
hücre
yayılım
olasılığı
üzerine
dikkat
çekildi
.
Aslında
malign
komplikasyonlara
göre
benign
komplikasyonlar
daha
sık
görülmektedir
,bunlar:
İatrojenik
endometriosis,
adenomiyozis,
parazitik leiomiyoma ve yaygın peritonel leiyomiyomatozis’dir (DPL) (28).
4.1. Parazitik Miyom
Parazitik
miyom,
uterustan
ayrılmış
ve
damarsal
kaynağını
diğer
oragnlardan
alan
miyomdur
(29).
Sistematik
derlemede,
parazitik
miyom
ve
uterin
cerrahi
arasındaki
ilişki
araştırlımıştır
(30).
274
parazitik
miyom
vakasının
120’sinin
(%44)
geçirilmiş histerektomi veya miyomektomi öyküsü vardı; bunların %90’ında morselasyon uygulanmıştı.
48
aylık
takip
sonrası;
Morselasyonlu
laparoskopik
hiserektomi
sonrası
parazitik
miyom
insidansı
%0,12-0,95
ve
morsellasyonlu
laparoskopik
miyomektomi
sonrası
insidans
ise
%0,2-1,25
tir
(31).
Genel
semptomlar
karın
ağrısı
(%49),
abdominal
bası
veya
kitle
(%11),
vajinal
kanama
(%10)
ve
abdominal
distansiyondur
(%5)
(30).
Genellikle
parazitik
miyomlar laparoskopik çıkartılabilir.
4.2. Adenomiyozis
Donnez
ve
ark.
laparoskopik
subtotal
histerektomi
uygulanmış
1613
kadının
9
‘unda
operasyon
sonrası
adenomiyozis
(%0,56)
tespit
etmişlerdir.
Lezyonlar
serviks
ve
uterosakral
ligamentlerden
ayrı
olarak
lateral
ve
retroservikal
boşluklarda
bulunmaktadır.
Ana
semptomlar
pelvik
ağrı
ve
disparoni
olarak
tespit
edilmiştir.
Lezyonlar
laparoskopik
olarak
rektum
ve
pararektal fossa disseksiyonu ile çıkartılmıştır(32).
4.3. Endometriozis
Diğer
benign
komplikasyonlardan
biri
de
iatrojenik
endometriozistir.
Semptomlar
pelvik
ağrı,
abdominal
distansiyon
ve
üriner
semptomlar
olup
,cerrahiden
6
ay
ile
7
yıl
sonrasında
görülebilir.
Schuster
ve
ark.
(33)
morselasyonlu
laparoskopik
subtotal
histerektomili
277
hasta
ile
abdominal/vajinal
histerektomili
187
hastayı
karşılaştırmıştır.
Benign
endikasyon
nedeniyle
16
kadın
(%3.5)
ikinci
operasyona
alınmıştır.
Vakaların
%1,4’ünde
endometriozis
tespit
edilmiş,
morsele
edilen
ve
morsele
edilmeyen
grupta
fark
saptanmamıştır.Endometriozis
odakları
pelvis,
vajinal
kubbe,
sigmoid
kolon
veya
trokar
yerinde görülmüştür (28).


TJODist
Bülteni

TJOD
İstanbul Şubesi
4.4. Yaygın peritoneal leiyomiyomatozis (DPL)
DPL,
periton
ve
omentumda
birçok
düz
kas
tümörünün
implantasyonudur
.
Etiyoloji
belirsiz
olsa
da,
metaplastik
subperitoneal
mezenkim
hücrelierinin
hormonal
yanıtı
nedeniyle
oluştuğu
düşünülmektedir
(34,35).
DPL
nadir
(%0,57)
olup
tedavisi
tartışmalıdır
(36).
GnRH
analogları
ile
ovaryan
supresyonun
lezyon
boyutunu
küçülttüğü
gösterilmiş
olsa
da
debulking
cerrahi
ile
omentektomi
en
iyi
alternatif
olarak
kabul
edilmektedir.
Cerrahiye
rağmen
rekürrensler
bildirilmiştir
(37).
5. Klinik Pratikte Değişiklikler
Enerjili
morselasyon
kullanımı
ile
ilgili
medikal
ve
medikolegal
endişeler
nedeniyle,
minimal
invaziv
cerrahide
uygulanan
tekniklerin
maliyeti
karşısında
laparotomik
miyomektomi
ve
histerektomide
artış
vardır.
669
jinekolog
ile
yapılan
bir
çalışmada
enerjili
morselasyon
oranının
dramatik
şekilde
azaldığı
görülmektedir
(38).
FDA
uyarısından
önce
%85
‘i
enerjili
morselasyon
yaparken,
sonrasında
%71’i
histerektomi
ve
miyomektomi
sırasında
enerjili
morselasyonu
bıraktıklarını
bildirmişlerdir. Ayrıca jinekologların %45’i laparotomi oranlarının arttığını bildirmişlerdir.
Harris
ve
ark.
FDA
uyarısının
öncesi
ve
sonrasında
histerektomi
yöntem
ve
komplikasyonlarını
değerlendirmişlerdir
(39).
FDA
uyarısı
sonrasında
laparoskopik
cerrahide
%4.1
azalma,
komplikasyon
oranında
artış
(%2,2-2,8,
P=0,015)
ve
hastaneye
yeniden
yatış
oranında
artış
(%3,4-4,2,
P=
0,025)
saptamışlardır.
Diğer
çalışmalarda
laparoskopik
histerektomi
benign vakalarda %8,7 azalırken, laparoskopik miyomektomi %19 oanında azalmıştır(40).
Cerrahi
yöntem
seçilirken,
mortalite,
morbidite
ve
yaşam
kalitesi
değrlendirilmeli,
kar-zarar
hesaplanmalıdır.
Sidehoff
ve
ark.
Laparotomi
ile
histerektomi
veya
laparoskopik
histerektomi
ve
morselasyon
yapılmış
100000
kadından
oluşan
varsayımsal
kohort
çalışmasında
klinik
sonuçları
değerlendirmişlerdir
(41).
Laparoskopik
histerektomide
transfüzyon,
yara
yeri
enfeksiyonu,
venöz
tromboemboli
ve
insizyonel
herni
oranlarında
düşme
ve
yaşam
kalitesinde
artış
olacağını
göstermişlerdir.
Ancak
laparoskopik
histerektomi
ve
morselasyon
yapılan
grupta
leiyomiyosarkomdan
kaynaklanan
ölüm
oranı (86 vs 71/100.000) ve total mortalite oranı daha yüksek (98 vs 103/100.000) bulunmuştur .
6. Kapalı Sistemde Yapılmayan Morselasyona Alternatif Teknikler
Minimal
invaziv
yöntemleri
terk
etmeden
doku
yayılımını
engellemek
için
pekçok
yöntem
önerilmiştir.
Bu
yöntemlerden
biri
kapalı
sistem
morselasyonudur.
Diğeri
ise
morselasyon
yerine,
büyük
spesmen
abdominal
kavite
içinde
ikiye
bölünebilir
veya
sirküler
şekilde
kesilip
birkaç
parçaya
ayrılabilir
(42).
Daha
sonra
bu
spesimenler
de
vajinal
kolpotomi
veya
mini
laparotomi ile alınabilir.
Pekçok
yazar
kapalı
sistem
morselasyonunun
kolaylıklarını
bildirmiştir
(43-46).
Winner
ve
ark.
kapalı
sistemde
yapılmayan
ve
kapalı
sistemde
yapılan
moraselasyonun
perioperatif
komplikasyonlarını
karşılaştırmıştır
(47).
Perioperatif
komplikasyonlar
benzer
iken
kapalı
sistem
cerrahisi
diğer
yöntemden
20
dakika
uzun
sürmüştür
(47).
Vargas
ve
ark
da
benzer
sonuç
bulmuştur
(48).
274
kadından
oluşan
başka
bir
çalışmada
enerjili
morselasyon
uygulanan
laparoskopik
miyomektomi
ve
histerektomi
yapılan
olgular,
mini
laparotomi
veya
vajinal
histerektomi
ve
myomektomi
sonrası
manuel
morselasyon
uygulanan
olgular
ile
karşılaştırlımıştır(48).
Perioperatif
komplikaysonlar
benzer
olsa
da
mini
laparotomili
manuel
morselasyon
,laparoskopik
enerjili
morselasyona
göre
daha
kısa
operasyon
süresiyle
ilişkili
(140,5
dk
vs.
164,2
dk,
p= 0,05) bulunmuştur.
Kapalı
sistemli
morselasyon
popüler
olmaya
başlamıştır
.
Ancak
,kapalı
sistemle
morselasyonda
torbadan
dışarıya
sızıntı
olabilir.
Enerjili
morselasyon
yapılan
76
kadından
oluşan
bir
çalışmada,
7
kadında
doku
veya
boya
sızıntısı
izlenmiştir
(%9,2)
(50).
Endoskopik
morselasyon
torbalarının
güvenilirliğini
araştıran
başka
bir
çalışmada
,
kapalı
sistem
ile
transvajinal
morselasyon
yapılan
laparoskopik
histerektomili
olgularda
4
hastada
(%33)
metilen
mavisi
sızıntısı
tespit
etmişlerdir (51).
7. Sonuç
Kapalı
sistem
ile
yapılmayan
morselasyon
daha
düşük
sağkalım
oranlarıyla
ilişkilidir.
Uterus
ve
miyom
morselasyonu
iatrojenik
endometriosis,
parazitik
miyom
ve
nadiren
DPL
ye
sebep
olabilir.
Bu
benign
komplikasyonlar
sarkomatöz
dokunun
yayılmasından
daha
sık
görülür.
Bu
yüzden
kapalı
sistem
morselasyon
pratiği
geliştirilmelidir.
Abdominal
kavitede
doku yayılımı engellemek için minimal invaziv teknikler kullanılmalıdır. Daha ideal teknik ve aletler gelişecektir.
Makalenin linki:
https://www.ncbi.nlm.nih.gov/pubmed/28159054


TJODist
Bülteni

TJOD
İstanbul Şubesi
Gebelik
sırasında
tiroid
glandı
boyutları
iyotun
yeterli
olduğu
ülkelerde
%10
oranında,
iyot
yetersizliği
olan
bölgelerde
ise
%20-40
oranında
artar.
Tiroksin
(T4)
ve
triiyodotironin
(T3)
üretimi
yaklaşık
%50
oranında
artarken,
günlük
iyot
gereksinimi
de %50 oranında artmaktadır.
Bu
fizyolojik
değişiklikler
sağlıklı
kadınlarda
sorunsuz
olarak
gerçekleşirken
altta
yatan
tiroid
patolojileri
varlığında
gebelikte
tiroid
disfonksiyonu
ile
sonuçlanabilir.
Bununla
birlikte,
gebelik
sırasında
maternal
(ve
fetal)
tiroid
fonksiyonlarının
değerlendirilmesi
güçtür
ve
laboratuvar
testlerinin
yorumlanması
gebe
olmayanlardan
farklıdır.
Özellikle
erken
gebelikte
plasental hCG tiroid hormon sekresyonunu uyarır ve sıklıkla TSH düzeylerinin azalmasına neden olur.
Maternal
TSH
düzeylerinin
geçici
olarak
baskılanması
sık
görülür
ve
güvenli
olduğu
düşünülmektedir;
bununla
birlikte,
serum
TSH
için
referans
üst
sınırı
tartışmalıdır.
Ek
olarak,
gebelerin
yaklaşık
%18’inde
tiroid
peroksidaz
antikoru
(TPOAb)
ya
da
tiroglobulin
antikoru
(TgAb)
pozitiftir.
TPOAb
pozitifliğinin
gebelik
sırasında
olumsuz
etkilerinin
olduğuna
ilişkin
veriler
mevcuttur ve tiroid antikor pozitifliğinin postpartum dönemde tiroid disfonksiyonu riskini arttırdığı da bilinmektedir.
Gebelik
döneminde
Graves’
hastalığının
(GD)
yönetimi
de
maternal
antikorlarla
birlikte
antitiroid
ilaçların
maternal
ve
fetal
tiroid
fonksiyonları
üzerindeki
farklı
etkileri
ve
olası
teratojenik
etkileri
nedeniyle
güçtür.
Hafif
hipertiroidi
anne
için
güvenli
olmakla
birlikte,
orta
ve
ağır
derecede
hipertiroidi
tehlikelidir.
Tiroid
disfonksiyonun
prevalansı
ve
olası
olumsuz
etkileri
gebelik
öncesi
ya
da
sırasında
tiroid
fonksiyonlarının
universal
olarak
değerlendirilmesi
önerilerini
gündeme
getirmekle
birlikte taramanın maliyet, etkinlik ve pratikteki etkilerini de dikkate alan çalışmaların sonuçları değişkendir. Bu kılavuzda,
Amerikan
Tiroid
Cemiyeti’nin
(ATA)
2011
kılavuzunda
yer
alan
öneriler
yeni
bilgiler
ışığında
güncellenmiş
ve
aşağıda
özetlenmiştir:
Tiroid fonksiyon testleri ve gebelik
•
Mümkünse
serum
TSH
düzeyleri
için
lokal
popülasyon
verileriyle
belirlenen
trimester-spesifik
referans
aralıkları
kullanılmalıdır.
Referans
aralıklarının
belirlenmesi
için
sadece
bilinen
tiroid
hastalığı
olmayan,
iyot
alımı
optimal
olan
ve TPOab negatif olan gebe kadınların verileri kullanılmalıdır.
•
Lokal
popülasyon
verilerinin
bulunmadığı
hallerde,
ilk
trimesterde
(7.-12.
haftalar
arasında)
alt
sınır
yaklaşık
0.4
mU/L,
üst
sınır
ise
yaklaşık
0.5
mU/L
azaltılabilir.
İkinci
ve
üçüncü
trimesterde
ise
yavaş
yavaş
gebelik
dışı
düzeylere
döner.
•
Serum
FT4
düzeylerinin
indirekt
analog
immunoassay
ile
ölçümü
gebelikten
etkilenir
ve
üretici
firmaya
göre
değişkenlik gösterir. Gebelerde kullanılan metoda ve trimestere özgü referans aralıkları kullanılmalıdır.
•
Gebeliğin
son
döneminde
FT4
yerine
TT4
ölçümü
(gebeliğe
spesifik
referans
aralıklarıyla)
güvenilir
bir
yöntemdir.
FT4 konsantrasyonlarının tahmini FT4 indeksi hesaplanarak da yapılabilir.
İyot durumu ve nütrisyon
•
•
Medyan
üriner
iyot
konsantrasyonları
(UIC)
popülasyonların
iyot
yeterliliğinin
değerlendirilmesi
için
kullanılabilir,
ancak tek spot ölçüm ya da 24 saatlik UIC kişilerin iyot yeterliliğinin değerlendirilmesi için uygun yöntemler değildir.
•
Tüm
gebeler
günde
yaklaşık
250
mcg
iyot
almalıdır.
Bulunulan
ülkeye
göre
250
mcg
iyot
alımını
sağlamak
için
stratejilerin değiştirilmesi gerekebilir.
•
ABD
dahil
pek
çok
bölgede
gebelik
planlayan
ya
da
gebe
kadınların
diyetlerini
potasyum
iyodat
formunda
150
mcg
iyot ile desteklemeleri gerekir. Optimal olarak gebelikten 3 ay önce başlanmalıdır.
•
Düşük
gelir
düzeyi
olan
ülkelerde
ve
tuzun
iyotla
zenginleştirilmediği
ya
da
iyot
desteklerinin
bulunmadığı
bölgelerde
doğurganlık
çağındaki
kadınlara
ve
gebelere
senede
bir
kez
yaklaşık
400
mg
iyodize
yağ
verilebilir.
Bu
geçici
bir
önlemdir; uzun dönem strateji olarak uygulanmamalıdır ve diğer seçeneklerin varlığında kullanılmamalıdır.
Gebelik Sırasında ve Postpartum Dönemde Tiroid Hastalıklarının Tanısı ve
Yönetimi - Amerikan Tiroid Cemiyeti 2017 Kılavuz
Erik K. Alexander, Elizabeth N. Pearce, Gregory A. Brent, Rosalind S. Brown, Herbert Chen, Chrysoula Dosiou, William A.
Grobman, Peter Laurberg, John H. Lazarus, Susan J. Mandel, Robin P. Peeters, and Scott Sullivan
Özetleyerek tercüme eden: Dr. Hande Yağmur,
Koç Üniversitesi Hastanesi Kadın Hastalıkları ve Doğum Kliniği


TJODist
Bülteni

TJOD
İstanbul Şubesi
•
Hipertiroidi tedavisi gören ya da LT4 alan gebelerin iyot desteğine ihtiyacı yoktur.
•
Gebelikte
GD
cerrahi
tedavisine
hazırlık
dışında
aşırı
miktarda
iyot
maruziyetinden
kaçınılmalıdır.
Yüksek
dozda
iyot
maruziyetine yol açan ilaç ve diyagnostik testler istenirken risk/yarar dengesi dikkate alınmalıdır.
•
Fetal
tiroid
disfonksiyonu
riski
nedeniyle
gebelik
sırasında
diyet
ve
besin
destekleriyle
günde
500
mcg
üzerinde
iyot
alımından kaçınılmalıdır.
•
Tiroid otoantikorları ve gebelik komplikasyonları
•
TPOAb
ya
da
TgAb
pozitif
olan
ötiroid
gebelerde
gebelik
konfirme
edildiğinde
ve
midtrimestere
kadar
her
4
haftada
bir TSH bakılmalıdır.
•
TPOAb pozitif gebelerde selenyum desteği önerilmemektedir.
•
Tekrarlayan gebelik kaybı öyküsü olan ötiroid kadınlarda intravenöz immünglobülin tedavisi önerilmemektedir.
•
TPOAb
pozitif
ötiroid
gebelerde
LT4
tedavisinin
gebelik
kaybı
riskini
azalttığına
dair
kanıtlar
yetersizdir.
Ancak,
gebelik
kaybı
öyküsü
olan
TPOAb
pozitif
ötiroid
gebelere
minimal
riske
karşın
potansiyel
yararı
nedeniyle
LT4
verilmesi düşünülebilir. Bu vakalarda, uygun LT4 başlangıç dozu 25-50 mcgdır.
•
Preterm
doğumların
önlenmesi
için
tiroid
otoantikorları
pozitif
ötiroid
gebelerde
LT4
tedavisine
ilişkin
kanıtlar
yetersizdir.
Tiroid hastalıklarının infertilite ve ART üzerine etkisi
•
İnfertilite nedeniyle başvuran her kadında TSH düzeyi değerlendirilmelidir.
•
Gebelik isteyen ve klinik hipotiroidisi olan infertil kadınlarda LT4 tedavisi önerilmektedir.
•
Doğal
konsepsiyon
deneyen
(ART
yapılmayan),
subklinik
hipotiroidisi
olan
ve
tiroid
antikorları
negatif
olan
kadınlarda
LT4
tedavisinin
fertiliteye
olumlu
etki
ettiğine
dair
kanıtlar
yetersizdir.
Ancak,
gebelik
elde
edilmesi
halinde
hipotiroidinin
progresyonunu
önleyebileceği
için
verilmesi
düşünülebilir.
Ek
olarak
düşük
doz
(25-50
mcg/gün)
LT4
tedavisi minimal risk taşımaktadır.
•
Doğal
konsepsiyon
deneyen
(ART
yapılmayan),
tiroid
antikorları
pozitif
ötiroid
kadınlarda
LT4
tedavisinin
fertiliteye
olumlu etki ettiğine dair kanıtlar yetersizdir. Bu nedenle, LT4 tedavisi önerilmemektedir.
•
IVF
ya
da
ICSI
yapılan
ve
subklinik
hipotiroidisi
olan
kadınlara
LT4
tedavisi
verilmelidir.
Tedavinin
amacı
TSH
düzeyinin <2.5 mU/L olmasıdır.
•
Tiroid
antikorları
pozitif
ötiroid
kadınlarda
LT4
tedavisinin
ART
başarısına
olumlu
etki
ettiğine
dair
kanıtlar
yetersizdir.
Ancak,
potansiyel
olumlu
etkileri
yanında
riskin
de
minimal
olması
nedeniyle
verilmesi
düşünülebilir.
Bu
vakalarda,
uygun LT4 başlangıç dozu günde 25-50 mcgdır.
•
ART uygulanan tiroid otoantikorları pozitif ötiroid kadınlarda glukokortikoid tedavisi önerilmemektedir.
•
Tiroid
fonksiyon
testleri
mümkünse
kontrollü
ovaryan
hiperstimülasyon
(KOH)
öncesinde
ya
da
1-2
hafta
sonrasında
yapılmalıdır çünkü KOH sırasında yapılan testlerin yorumlanması güç olabilir.
•
KOH
sonrasında
gebelik
elde
eden
kadınlarda
TSH
yüksekliği
hipotiroidi
ve
gebelik
bölümünde
yer
alan
öneriler
uyarınca
tedavi
edilmelidir.
KOH
sonrasında
hafif
TSH
yüksekliği
olan
gebe
olmayan
kadınlarda,
2-4
hafta
sonra
TSH düzeyleri kontrol edilmelidir çünkü normal düzeylere dönebilir.
Hipotiroidi ve gebelik
•
Gebelikte maternal hipotiroidi TSH düzeyinin gebeliğe spesifik üst sınırın üzerinde olması şeklinde tanımlanır.
•
Gebeliğe özgü TSH referans aralıkları şu şekilde tanımlanmalıdır:
•
Mümkünse
popülasyon-
ve
trimester-spesifik
referans
aralıkları
hizmetin
verildiği
tipik
popülasyonu
yansıtacak
şekilde
hizmetin
verildiği
kurum
ya
da
laboratuvar
tarafından
belirlenmelidir.
Sağlıklı,
iyot
alımı
optimal,
TPOAb
negatif ve tiroid hastalığı olmayan gebelerde tanımlanmalıdır.
•
Eğer
mümkün
değilse,
benzer
hasta
popülasyonunda
ve
benzer
TSH
ölçüm
yöntemleri
kullanılarak
belirlenen
referans aralıkları dikkate alınmalıdır.
•
Bu
iki
seçeneğin
mevcut
olmadığı
hallerde,
TSH
üst
sınırı
olarak
yaklaşık
4.0
mU/L
kullanılabilir.
Çoğu
ölçüm
yöntemi için bu sınır gebe olmayan kadınlarda kabul edilen üst sınırdan yaklaşık 0.5 mU/L düşüktür.
•
Gebelikte klinik hipotiroidinin tedavisi önerilmektedir.
•
TSH düzeyi >2.5 mU/L olan gebelerde TPOAb değerlendirilmelidir.
•
Gebelikte subklinikte hipotiroidiye yaklaşım şöyle olmalıdır:
(a) LT4 tedavisi şu hastalar için önerilmektedir:
•
TSH düzeyi gebelik için sınırın üzerinde olan TPOAb pozitif kadınlar
•
TSH düzeyi >10 mU/L olan TPOAb negatif kadınlar
(b) LT4 tedavisi şu hastalar için düşünülebilir:


TJODist
Bülteni

TJOD
İstanbul Şubesi
•
TSH düzeyi > 2.5 mU/L ve gebelik için üst sınırın altında olan TPOAb pozitif kadınlar
•
TPOAb negatif kadınlar ve TSH düzeyi gebelik için üst sınırın üzerinde ve <10 mU/L olan TPOAb negatif kadınlar
(c)
LT4 tedavisi şu hastalar için önerilmemektedir:
•
TSH düzeyi normal (gebeliğe özgü referans aralığında ya da <4.0 mU/L) TPOAb negatif kadınlar
•
İzole hipotiroksinemi gebelikte rutin olarak tedavi edilmemelidir.
•
Maternal
hipotiroidi
için
önerilen
oral
LT4
tedavisidir.
T3
ya
da
tiroid
ekstresi
gibi
diğer
preparatlar
gebelikte
kullanılmamalıdır.
•
Genel
popülasyondaki
hipotiroidi
tedavisine
paralel
olarak
gebelikte
de
TSH
düzeylerini
trimester-spesifik
referans
aralığının
düşük
yarısında
tutmak
hedeflenmelidir.
Gebeliğe
özgü
referansların
bulunmaması
halinde
maternal
TSH
düzeyinin 2.5 mU/L altında tutmak hedeflenir.
•
Klinik
ve
subklinik
hipotiroidisi
olan
kadınlarda
(tedavi
alan
ya
da
almayan)
ya
da
hipotiroidi
riski
olan
kadınlarda
(örneğin,
ötiroid
ancak
TPOAb
ya
da
TgAb
pozitif,
post-hemitiroidektomi,
ya
da
radyoaktif
iyot
tedavisi
görmüş
kadınlar) TSH düzeyleri midgestasyona kadar her 4 haftada bir ve 30 haftaya yakın en az bir kez kontrol edilmelidir.
•
Reprodüktif
çağda
hipotiroidi
tedavisi
gören
kadınlara
gebelikte
LT4
ihtiyacını
artabileceği
bilgisi
verilmelidir.
Ayrıca
gebelik şüphesinde ya da doğrulandığında hekimleriyle iletişime geçmeleri önerilmelidir.
•
Gebelik
planlayan
ve
LT4
tedavisi
alan
kadınlarda
prekonsepsiyonel
dönemde
TSH
bakılmalı
ve
LT4
dozu
TSH
düzeyi alt sınır ile 2.5 mU/L arasında olacak şekilde ayarlanmalıdır.
•
LT4
kullanan
hipotiroidili
kadınlar
gebelik
şüphesi
ya
da
doğrulanması
halinde
hekime
başvurmaksızın
LT4
dozunu
yaklaşık
%20-30
oranında
arttırmalı
ve
en
kısa
zamanda
değerlendirme
için
hekimiyle
iletişime
geçmelidir.
Mevcut
günlük LT4 dozuna haftada iki tablet eklenmesiyle önerilen doz artışı sağlanabilir.
•
Doğum
sonrasında
LT4
dozu
gebelik
öncesinde
kullanılan
doza
düşürülmeli
ve
yaklaşık
6
hafta
sonra
tiroid
fonksiyon testleri değerlendirilmelidir.
•
Gebelik
sırasında
LT4
başlanan
bazı
kadınlarda
postpartum
dönemde
LT4
ihtiyacı
kalmayabilir.
Özellikle
günlük
LT4
dozunun
<50
mcg
olduğu
kadınlarda
LT4
kesilebilir.
LT4
tedavisinin
kesilmesine
hasta
ve
hekim
birlikte
karar
vermelidir ve kesilmesi halinde 6 hafta sonra TSH kontrol edilmelidir.
•
Yeterince
tedavi
edilen
hipotiroidili
gebelerde
tiroid
fonksiyonlarının
değerlendirilmesi
dışında
ek
maternal
ya
da
fetal
testlere
(fetal
ultrasonografi
takibi,
antenatal
testler,
ve/veya
umbilikal
kan
örneklemesi)
gerek
yoktur.
Sadece
I131
ablasyon ya da cerrahi tedavi yapılan ve GD olan kadınlarda TSH reseptör antikorlarının (TRAb) izlenmesi gerekir.
Gebelikte tirotoksikoz
•
lk
trimesterde
serum
TSH
düzeylerinin
suprese
olması
halinde,
detaylı
öykü
ve
fizik
muayenenin
yanında
serum
FT4
ya da TT4 düzeyleri bakılmalıdır. TRAb ve TT3 tirotoksikoz etyolojisinin aydınlatılmasına yardımcı olabilir.
•
Gebelikte radyonüklid sintigrafi ya da radyoiyot ‘uptake' testleri yapılmamalıdır.
•
Gestasyonel
geçici
tirotoksikoz
ve/veya
hiperemezis
gravidaruma
bağlı
anormal
tiroid
testleri
varlığında
destek
tedavisi
yapılmalı,
dehidratasyon
giderilmeli
ve
gerekirse
hastaneye
yatırılmalıdır.
Antitiroid
ilaçlar
(ATD)
önerilmemektedir, ancak beta-blokerler düşünülebilir.
•
Tirotoksikozu
olan
reprodüktif
çağdaki
kadınlarla
gebelik
olasılığı
tartışılmalıdır.
GD
olan
ve
gebelik
planlayan
kadınlar
ATD’ların
teratojenik
etkileri
de
dahil
olmak
üzere
hastalığın
gebelik
sırasındaki
yönetiminin
kompleks
olduğu
hakkında
bilgilendirilmelidir.
Prekonsepsiyonel
dönemde
tüm
tedavi
seçeneklerinin
riskleri
ve
yararları
anlatılmalıdır
•
Tirotoksikozu
olan
kadınlar
gebelik
öncesinde
ötiroid
hale
getirilmelidir.
Farklı
avanatajlara
ve
risklere
sahip
tedavi
seçenekleri vardır ve bu seçenekler arasında I131 ile ablasyon, tiroidektomi ya da ATD ile tedavi yer almaktadır.
•
Metimazol
(MMI)
ya
da
propiltiyourasil
(PTU)
kullanan
kadınlara
olası
gebelik
durumunun
en
kısa
zamanda
doğrulanması
gerektiği
anlatılmalıdır.
Gebelik
testinin
pozitif
olması
halinde
hekimleriyle
hemen
iletişime
geçmeleri
gerekir.
•
Antitiroid ilaçlar:
(a)
Erken
gebelik
döneminde,
düşük
doz
MMI
(<5-10
mg/d)
ya
da
PTU
(<100-200
mg/d)
ile
ötiroid
olan
GD’li
kadınlarda
olası
teratojenik
etkiler
nedeniyle
antitiroid
ilaçların
kesilmesi
düşünülebilir.
Bu
karar
verilirken
hastalık
öyküsü,
guatr
büyüklüğü,
tedavi
süresi,
son
tiroid
fonksiyon
testlerinin
sonuçları,
TRAb
düzeyleri
ve
diğer
klinik
faktörler dikkate alınmalıdır.
(b)
Antitiroid
ilaçların
bırakılmasını
takiben
maternal
ve
fetal
değerlendirme
için
maternal
tiroid
fonksiyon
testleri
(TSH,
FT4
ya
da
TT4)
ve
klinik
muayene
1-2
haftada
bir
yapılmalıdır.
Klinik
ve
biyokimyasal
olarak
ötiroid
kalması halinde test aralıkları ikinci ve üçüncü trimesterde 2-4 haftaya uzatılabilir.
(c)
Her
değerlendirmede,
konservatif
yaklaşıma
(antitiroid
ilaç
verilmeksizin)
devam
etme
kararı
hem
klinik
hem de biyokimyasal olarak değerlendirme sonrasında verilmelidir.
•
Antitiroid
ilaçların
kesilmesi
halinde
tirotoksikoz
riski
yüksek
olan
gebelerde
ilaçlara
devam
etmek
gerekebilir.

TJODist
Bülteni

TJOD
İstanbul Şubesi
Halihazırda
hipertiroid
olmak
ya
da
ötiroidinin
sağlanması
için
>5-10
mg/d
MMI
ya
da
>100-200
mg/d
PTU
gereksinimi tirotoksikoz için risk faktörleridir. Bu vakalarda;
(a) 16. haftaya kadar PTU önerilir.
(b) MMI kullanan ve tedaviye devam etmesi gereken kadınlarda en kısa zamanda PTU’e geçilmelidir.
(c) MMI’den PTU’e geçerken yaklaşık 1:20 doz oranı kullanılmalıdır (örneğin, 5 mg/d MMI = 100 mg/d PTU).
(d)
16.
haftadan
sonra
antitiroid
tedavi
gerekliyse,
PTU’e
devam
edilmesi
ya
da
MMI’e
geçilmesi
tartışmalıdır.
Her
iki
ilacın
potansiyel
olumsuz
etkileri
vardır
ve
değişim
kontrolün
bir
süre
bozulmasıyla
sonuçlanabilir;
dolayısıyla
değişim önerilmemektedir.
•
Tiroid fonksiyon testleri;
(a) Gebelikte ATD kullanan kadınlarda FT4/TT4 ve TSH yaklaşık her 4 haftada bir bakılmalıdır.
(b)
En
düşük
etkin
MMI
ya
da
PTU
dozları
kullanılmalı
ve
üst
sınırda
ya
da
referans
aralığının
orta
derecede
üzerinde FT4/TT4 düzeyleri hedeflenmelidir.
•
İzole
fetal
hipertiroidi
dışında
(GD
için
ablatif
tedavi
görmüş
olan
gebede
maternal
TRAb
nedeniyle
gelişen
fetal
hipertiroidi)
LT4
ve
ATD
kombinasyonu
(ATD
fetusta
hipertiroidiyi
tedavi
ederken
LT4
annenin
ötiroid
kalmasını
sağlar) kullanılmamalıdır.
•
Gebelikte
tiroidektomi
nadiren
gerekir
ve
gerektiğinde
optimal
zaman
ikinci
trimesterdir.
Maternal
TRAb
konsantrasyonunun
yüksek
olması
halinde
(referans
üst
sınırının
3
katından
fazla),
anneninin
tiroidektomi
sonrasında ötiroid olması halinde dahi fetus gebelik boyunca fetal hipertiroidi açısından yakın izlenmelidir.
•
2011’de yazılıp 2015’te revize edilen ACOG Committee on Obstetric Practice konsensus kılavuzuyla hem fikir olarak;
1) Gebelerde trimesterden bağımsız olarak cerrahi girişim gerekiyorsa yapılmalıdır.
2) Elektif cerrahi girişim doğum sonrasına ertelenmelidir.
3)
Münkünse,
acil
olmayan
cerrahi
girişimler
preterm
kontraksiyonlar
ve
spontan
abortusların
en
az
olduğu
ikinci trimesterde yapılmalıdır.
•
GD
olan
gebeye
acil,
tiroid
dışı
ameliyat
yapılması
gerektiğinde
ATD
ile
ötiroid
olması
halinde
ek
tedavi
gerekli
değildir. İhtiyaç olduğunda beta-blokerler kullanılmalıdır.
•
TRAb ölçümleri;
(a)
Ablasyon
(radyoaktif
iyot
ya
da
cerrahi)
ile
tedavi
edilmiş
GD
öyküsü
varsa,
erken
gebelikte
ilk
tiroid
fonksiyon testleri yapılırken TRAb da bakılması önerilir.
(b) Erken gebelikte TRAb konsantrasyonu yüksekse, 18-22 hafta arasında tekrarlanmalıdır.
(c) Erken gebelikte ölçülemez düzeyde ya da düşükse, tekrar bakılması gerekmez.
(d) Gebelik doğrulandığında GD için ATD kullanılıyorsa, TRAb bakılması önerilir.
(e) Midgestasyonda ATD gerekiyorsa, TRAb tekrar 18-22 hafta arasında bakılmalıdır.
(f)
Üçüncü
trimesterde
anne
ATD
kullanıyorsa
ya
da
18-22
haftada
TRAb
yüksekse,
30-34
hafta
arasında
neonatal ve postnatal izlemin planlanması açısından tekrar TRAb bakmak gerekir.
•
Gebeliğin
ikinci
yarısında
annenin
kontrolsüz
hipetiroidisi
varsa
ve
gebeliğin
herhangi
bir
dönemnde
TRAb
yüksek
(üst
sınırın
3
katından
fazla)
bulunmuşsa
fetal
izlem
gereklidir.
İzlemin
deneyimli
obstetrisyen
ya
da
maternal-fetal
tıp
uzmanı
ile
konsültasyon
önerilir.
İzlemde
kalp
hızı,
büyüme,
amniyotik
sıvı
volümü
ve
fetal
guatr
varlığı
değerlendirilir.
•
Kordosentez
nadiren
ve
uygun
koşullarda
yapılmalıdır.
ATD
alan
kadınlarda
fetal
guatr
saptanması
halinde
fetusun
hipertiroid ya da hipotiroid olduğunun belirlenmesi için gerekebilir.
•
Otonom
nodülden
kaynaklanan
hipertiroidi
için
ATD
veriliyorsa,
fetus
gebeliğin
ikinci
yarısında
guatr
ve
hipotiroidi
bulguları
açısından
izlenmelidir.
Maternal
FT4
ya
da
TT4
düzeylerini
üst
sınırın
ya
da
sınırın
orta
derecede
üzerinde
tutacak şekilde düşük ATD dozları kullanılmalıdır.
Gebelikte tiroid nodülü ve kanseri
•
Baskılanmış
TSH
düzeylerinin
16.
haftadan
sonra
da
persiste
etmesi
halinde,
tiroid
nodülünün
ince
iğne
aspirasyon
biyopsisi
(İİAB)
gebelik
sonrasına
ertelenebilir.
Bu
dönemde,
eğer
TSH
halen
baskılanmış
ise
ve
anne
emzirmiyorsa
radyonüklid inceleme yapılabilir.
•
Tiroid
nodülü
olan
gebelerde
kalsitonin
ölçümünün
yararı
bilinmemektedir.
Tiroid
nodülü
olan
gebelerde
rutin
kalsitonin ölçülmesi ya da ölçülmemesi önerilememektedir.
•
TSH
düzeyleri
baskılanmamış
olan
ve
gebelikte
yeni
tespit
edilen
tiroid
nodülleri
için
İİAB
genellikle
önerilir.
Hangi
nodüllerden
biyopsi
yapılması
gerektiğine
sonografik
özelliklere
göre
karar
verilmelidir.
İİAB
zamanlaması
(gebelik
sırasında ya da erken postpartum dönemde) kanser riski ve hastanın tercihine bağlıdır.
•
Radyonüklid sintigrafi ya da radyoaktif iyot ‘uptake’ testi gebelik sırasında yapılmamalıdır.
•
Sitolojik
olarak
benign
tiroid
nodülü
olan
gebelerde
gebelik
sırasında
özel
izlem
gerekmez
ve
2015
ATA
Tiroid
Nodülü
ve Diferansiye Tiroid Kanseri olan Erişkinler için Yönetim Kılavuzu uyarınca takip edilmelidirler.
•
Sitolojik
olarak
belirsiz
(önemi
belirsiz
atipi/önemi
belirsiz
foliküler
lezyon,
foliküler
neoplazi
için
şüpheli
ya
da


TJODist
Bülteni

TJOD
İstanbul Şubesi
malignite
için
şüpheli)
nodülü
olan
gebelerde,
sitolojik
olarak
malign
lenf
nodu
yoksa
ya
da
başka
metastatik
hastalık
bulgusu yoksa rutin olarak gebelik sırasında cerrahi girişim gerekmemektedir.
•
Sitolojik olarak belirsiz nodülde agresif davranış şüphesi varsa gebelik sırasında cerrahi girişim düşünülebilir.
•
Sitolojik olarak belirsiz nodüllerin değerlendirilmesi için gebelik sırasında moleküler testler önerilmemektedir.
•
Erken
gebelikte
tanı
koyulan
papiller
tiroid
karsinomu
(PTC)
sonografi
ile
izlenmelidir.
Eğer
24-26
haftadan
önce
önemli
büyüme
saptanırsa
ya
da
sitolojik
olarak
malign
servikal
lenf
nodları
varsa
gebelik
sırasında
cerrahi
girişim
düşünülmelidir.
Ancak,
midgestasyonel
döneme
kadar
stabil
kalırsa
ya
da
gebeliğin
ikinci
yarısında
tanı
koyulursa
cerrahi girişim doğum sonrasına ertelenebilir.
•
Gebeliğin
yeni
tanı
koyulan
medüller
karsinom
ya
da
anaplastik
kanser
üzerine
etkileri
bilinmemektedir.
Tedavide
gecikmenin
sonuçları
olumsuz
etkileme
olasılığı
yüksektir
ve
tüm
klinik
faktörlerin
değerlendirilmesini
takiben
cerrahi
girişim düşünülmelidir.
•
Tiroid
kanseri
olan
gebelerde
prekonsepsiyonel
dönemde
belirlenen
TSH
düzeyleri
hedeflenmelidir.
TSH
16-20
haftaya kadar yaklaşık 4 haftada bir ve 26-32 hafta arasında en az bir kez bakılmalıdır.
•
Terapötik radyoaktif iyot (I131) tedavisinden sonra gebelik 6 ay ertelenmelidir.
•
Tedavi
edilmiş
diferansiye
tiroid
kanseri
(DTC)
öyküsü
olan
gebelerde
tiroglobulin
ölçülemez
düzeyde
(tiroglobulin
otoantikorları
yokluğunda)
ve
gebelik
öncesinde
hastalığa
dair
biyokimyasal
ya
da
strüktürel
kanıt
yoksa
gebelik
sırasında ultrasonografi ve tiroglobulin ile izlem gerekmez.
•
İyi
diferansiye
tiroid
kanseri
olan
ve
tedaviye
biyokimyasal
ya
da
strüktürel
olarak
tam
olmayan
yanıt
söz
konusu
ya
da aktif rekürren ya da rezidüel hastalık varsa gebelik sırasında ultrasonografi ve tiroglobulin ile izlem yapılmalıdır.
•
Papiller
tiroid
mikrokarsinom
tanısı
almış
ve
aktif
izlemde
olan
gebelerde
her
trimesterde
maternal
tiroid
ultrasonografisi yapılmalıdır.
Fetal ve neonatal etkiler
•
Maternal
tiroid
hastalığı
öyküsü,
gebelik
sırasında
antitiroid
ilaç
(MMI/PTU)
kullanımı,
gebelikte
anormal
tiroid
fonksiyon testleri ya da TRAb varlığı neonatolog ya da pediatriste iletilmelidir.
•
Gebelikte
ağır,
progresif
ya
da
kompleks
tiroid
hastalığı
varlığı
doğum
öncesinde
neonatolog
ya
da
pediatriste
iletilmeli
ve
pediatrik
endokrinolog
ile
konsültasyon
düşünülmelidir.
Diğer
durumlar
hakkında
doğum
sonrası
kısa
dönemde bilgi verilebilir.
•
Tüm yenidoğanlar doğumdan 2-5 gün sonra hipotiroidi açısından taranmalıdır.
Tiroid hastalığı ve laktasyon
•
Maternal
hipotiroidi
laktasyonu
olumsuz
etkileyebileceğinden
laktasyonda
zorlanan
ve
başka
neden
bulunamayan
kadınlarda TSH bakılmalıdır.
•
Subklinik
ve
klinik
hipotiroidi
süt
üretimi
ve
‘let-down’
üzerine
olumsuz
etkileri
nedeniyle
laktasyon
dönemindeki
kadınlarda tedavi edilmelidir.
•
Maternal
hipetiroidinin
laktasyon
üzerindeki
etkisi
net
anlaşılamamıştır.
Bu
nedenle,
laktasyonun
iyileştirilmesi
amacıyla hipertiroidinin tedavisine yönelik öneride bulunulamamaktadır.
•
Laktasyon
sırasında
I131
kontrendikedir.
Gerektiğinde
emzirmeye
başlamadan
önce
3-4
gün
süreyle
sütlerin
sağılıp
atılması koşuluyla I123 kullanılabilir. Benzer şekilde, Tc-99m perteknetat uygulandığı gün süt sağılıp atılmalıdır.
•
Laktasyondaki kadınlarda hipertiroidi tedavisi kararı laktasyon döneminde olmayan kadınlardaki prensiplere dayanır.
•
Laktasyon
dönemindeki
kadınlarda
antitiroid
ilaç
endikasyonu
varsa,
hem
MMI
(maksimum
20
mg/d)
hem
de
PTU
(maksimum
450
mg/d)
kullanılabilir.
Hem
MMI
hem
de
PTU
süte
az
ancak
tespit
edilebilir
miktarlarda
geçtiği
için
en
düşük etkin doz tercih edilmelidir.
•
ATD
kullanan
kadınların
çocukları
rutin
pediatri
takiplerinde
büyüme
ve
gelişme
açısından
takip
edilmelidir.
Çocuklarda tiroid fonksiyonlarının değerlendirilmesi rutin olarak önerilmemektedir.
•
Tüm emziren kadınlar günde diyetle yaklaşık 250 mcg iyot almalıdır.
•
Emziren
kadınlar
ek
olarak
150
mcg
iyot
içeren
besin
desteği
almalıdır.
Optimal
olarak
potasyum
iyodür
şeklinde
(multivitamin
içinde)
verilmelidir
çünkü
‘kelp'
ve
diğer
su
yosunu
formlarıyla
tutarlı
miktarlarda
iyot
alımı
sağlanamamaktadır.
•
Ciddi
iyot
ekslikliği
olan,
tuzun
iyotlanmadığı
ve
günlük
besin
desteğinin
mümkün
olmadığı
düşük
gelir
düzeyine
sahip bölgelerde emziren kadınlara doğumdan sonra oral iyodize yağ formunda tek doz 400 mg iyot verilmelidir.
•
Emzirme
döneminde
bebekte
hipotiroidiye
yol
açma
riski
nedeniyle
günde
500-1100
mcg
aşan
miktarlarda
iyot
alımından kaçınılmalıdır.


TJODist
Bülteni

TJOD
İstanbul Şubesi
Postpartum tiroidit (PPT)
•
Postpartum depresyon dahil depresyon geçiren tüm hastalar tiroid disfonksiyonu açısından araştırılmalıdır.
•
Postpartum
depresyonun
tirotoksik
fazında
semptomatik
hastalar
beta-blokerler
ile
tedavi
edilebilir.
Tedavide
ilk
seçenek
semptomların
kontrol
altına
alınabildiği
minimum
dozda
olmak
üzere
laktasyonda
kullanımı
güvenli
olan
propranolol ya da metoprololdür. Tedavi genellikle birkaç hafta için gereklidir.
•
Postpartum depresyonun tirotoksik fazında antitiroid ilaçların kullanımı önerilmemektedir.
•
Tirotoksik
fazın
geçmesini
takiben
yaklaşık
4-8
hafta
içinde
(ya
da
yeni
semptomlar
gelişirse)
hipotiroid
faz
açından
tarama amacıyla TSH bakılmalıdır.
•
Postpartum
tiroidite
bağlı
semptomatik
hipotiroidisi
olan
kadınlarda
LT4
başlanması
düşünülmelidir.
Tedavi
başlanmaması
halinde,
tiroid
fonksiyonları
düzelene
kadar
4-8
haftada
bir
TSH
kontrol
edilmelidir.
Gebelik
planlayan
ve emziren hipotiroid kadınlara da LT4 başlanmalıdır.
•
Eğer
PPT
nedeniyle
LT4
başlanmışsa,
12
ay
sonra
kesilmesi
planlanmalıdır.
Gebelik
halinde
ya
da
gebelik
planlıyorsa LT4 dozunun azaltılmasından kaçınılmalıdır.
•
PPT öyküsü olan kadınlarda kalıcı hipotiroidi açısından yılda bir TSH bakılmalıdır.
•
Ötiroid
ve
tiroid
antikorları
pozitif
olan
kadınlarda
PPT’in
önlenmesi
için
LT4
ya
da
iyot
kullanımı
etkili
değildir
ve
önerilmemektedir.
Gebelik öncesinde ya da gebelikte tiroid fonksiyonları için tarama
•
Erken
gebelikte
anormal
TSH
düzeyleri
açısından
tarama
yapılması
ya
da
yapılmamasına
yönelik
öneride
bulunabilmek için yeterli kanıt yoktur.
•
ART
planlanan
ya
da
TPOAb
pozitifliği
bilinen
hastalar
dışında
gebelik
öncesinde
anormal
TSH
düzeyleri
açısından
tarama yapılması ya da yapılmamasına yönelik öneride bulunabilmek için yeterli kanıt yoktur.
•
Gebelerde düşük FT4 düzeyleri için tarama yapılması önerilmemektedir.
•
Tüm
gebeler
ilk
prenatal
vizitte
tiroid
disfonksiyonu
öyküsü
ve
hali
hazırda
tiroid
hormonu
(LT4)
ya
da
antitiroid
ilaç
(MMI, CM ya da PTU) kullanımı ya da kullanım öyküsü açısından sorgulanmalıdır.
•
Gebelik
planlayanlarda
ya
da
erken
gebelik
döneminde
klinik
değerlendirme
yapılmalıdır.
Aşağıdaki
risk
faktörlerinden herhangi birinin varlığında, TSH bakılması önerilmektedir:
1
.
Hipotiroidi/hipertiroidi öyküsü ya da tiroid disfonksiyonu semptom/bulguları varlığı
2
.
Bilinen tiroid antikoru pozitifliği ya da guatr olması
3
.
Baş/boyun bölgesine irradyasyon ya da tiroid cerrahisi öyküsü
4
.
>30 yaş
5
.
Tip 1 diyabet ya da diğer otoimmün hastalıklar
6
.
Gebelik kaybı, preterm doğum ya da infertilite öyküsü
7
.
>2 gebelik öyküsü
8
.
Ailede otoimmün tiroid hastalığı ya da tiroid disfonksiyonu öyküsü
9
.
Morbid obesite (BMI >40 kg/m2)
1
0
.
Amiodaron ya da lityum kullanımı, ya da yakın zamanda iyotlu kontrast madde verilmiş olması
1
1
.
Orta-ağır derecede iyot eksikliği olduğu bilinen bölgelerde yaşıyor olmak
Ücretsiz tam metin erişim bağlantısı: http://online.liebertpub.com/doi/pdfplus/10.1089/thy.2016.0457


TJODist
Bülteni